原生生物情報サーバ
| 原生生物学情報
| DataBook
| 実験プロトコル
ゾウリムシにおける接合の誘導法
ゾウリムシが示す最も顕著な反応は接合(有性生殖)であろう。教科書などにも,接合対の写真が紹介されていることが多い。接合対は,野外からゾウリムシを採集してきた際,採集された数が多いときにはサンプルの中に接合している最中のものが見つかることがある。また,採集してきた細胞を適当な培養液中で飼育していると,ときたま接合対がみつかることもある。
しかし,実習や研究の目的で,任意の日時に,必要なだけの接合対を得るためには,以下の方法でクローン化した株を培養・維持しなければならない。
接合前の準備
クローニング
ゾウリムシには,雄・雌に相当する「接合型」とよばれる性のちがいがある。異なる接合型の細胞を一緒にするとお互いの間で接合が起こる。したがって,自らの望みの時に接合を誘導するためには,あらかじめ異なる接合型のものを別々にわけて培養しておく。
その方法とは・・・
細胞をマイクロピペットで「つまんで」単離したものを培養してクローン化する。

細胞の培養
接合誘導法には,通常の交配反応による接合誘導以外にも化学試薬処理による誘導などいくつかの方法がある(文献参照)。しかし,いずれの場合でも,基本的には交配反応活性の強い細胞を用いなければうまくいかない。そのための,すなわち交配反応活性の強い細胞を得るための培養法とは・・・
望ましい培養法
培養のステージ(対数増殖期,定常期など)によって細胞の生理的状態は変化し,接合型活性は定常期の初期〜中期にのみ現われる。そのため,交配反応を行なわせるためには,培養している細胞が現在どの培養ステージにあるかを常に把握できていなければならない。
従って,望ましい培養法としては,培養の対数増殖期と定常期がハッキリ区別できる培養条件が必要となる。この条件をみたすものが,試験管培養である。

試験管培養では,毎日,細胞が食いつくせるだけの餌を与え,常に翌日には定常期に達するようにできる。増殖速度の遅い株なら餌を少なめに,速いものには多めに与える。コンタミ(contaminationの略語;餌以外の雑菌)が目立つようなら,時折,抗生物質で処理するなり対処する等々して,各々の株が接合型活性を発現するのに最適な状態になるように調整する。望みの日時に細胞を接合の最適条件にすることが可能である。(餌を与えた後の増殖期は培養液が濁っているが,餌を食べ尽くし定常期に達すると透明に替わる。)
一方,フラスコ培養は,あらかじめ一定量の培養液のなかに細胞を移植して培養する。したがって,何日か後に定常期に達することになるが,それがいつかは株の増殖速度の違いやコンタミの程度などにより著しく差がでてくる(予測することが難しい)。同じ株でもコンタミが多い場合は,コンタミの影響で増殖速度が落ちて定常期に達するのが遅れたり,あるいは,ゾウリムシよりもコンタミバクテリアの方が増殖速度が速いので,定常期に達する頃には増え過ぎたコンタミの影響で細胞の元気が悪くなり,接合型活性がまったく出現しないことなどもよくある。
フラスコ培養で,接合型活性の強い細胞を得るには,雑菌(コンタミ)の極めて少ない,かつ,増殖速度の高い株でないと難しい。しかし,不可能ではない!
接合誘導に利用される培養液の種類
(具体的な作成法については各種文献を参照せよ。)
候 補 特 徴
レタスジュース ゾウリムシの研究者に多い。
新鮮な葉レタスから作る。時間がかかる。コスト高
ジュース原液は3日間の間欠滅菌,冷所保存
濁った培養液なので,使用前のコンタミの有無確認が困難
(作り方:文献参照)
アカエンドウマメ 筆者(月井雄二)の考案によるレタスジュース培養の変法
原液の作成・保存が楽(オートクレーブ,室温保存)。経済的。
培養液は透明なので使用前のコンタミの有無が
容易に確認できる。
(作り方:マメ40gを800mlの水にいれ,エタノールに溶かした
5mg/mlのスティグマステロールを4ml加える。)
これを滅菌し原液として室温保存。使用の際は,
上澄みを8枚位重ねたガーゼを通して瀘過,水を加えてもとの800mlに
調整する。その100mlに水,ドリル氏原液
を加え滅菌する(後は,使用時まで室温保存)。
滅菌前は懸濁しているが,ドリル氏液とともに滅菌する
と茶褐色の透明な液体になる。従って,使用前のコンタミ
の有無が容易に確認できる(濁れば雑菌が混入したことに
なる)。
使用前日に餌のバクテリアと塩化カルシウムを加え,
一晩培養する。
セロフィル ヒメゾウリムシの研究者に多い。
セロフィルはなかなか手に入りにくい(輸入品)。
(作り方:文献参照)
キナコ上澄 簡単に手に入る材料として勧められる。
細胞内に顆粒が増え,不透明になるのが玉にきず。
分裂速度,細胞密度,接合型活性はレタス,アカエンドウ
などと同様。
(作り方:キナコ1gを1000mlの水にけん濁させる。
しばらく静置した後,沈澱ができるだけ混じらないように
して上澄みをガーゼに通し,これにドリル氏原液を加え
滅菌する。)
メモ:
滅菌キナコ培養で培養すると,細胞内顆粒が増加し,
不透明になるので透過光観察の場合,細胞は黒ずんで
見える。このことを応用してホモ・ヘテロ接合対の識
別が可能(月井,198*)。
|
付記:
いずれも,滅菌が必要。
(理由:富栄養のため滅菌しないと雑菌のほうが先に増えてだめになる。)
ワラの煮汁などはあまり研究には使われていない。
しかし,株の保存用として,長期間手入れせずに保存がきくとして採用しているところもある。
☆★☆★ 滅菌装置がない,滅菌の手間がかけられない場合は?
考えられる方法
キナコ+フラスコ培養
上記のキナコ上澄み培養液を滅菌せずに用いる。なるべく大きな顆粒は除いた方がよいが,滅菌する場合に比べれば,大きめの顆粒成分が混じってもそれほど気にする必要はない。これにゾウリムシを入れて培養する。
フラスコ培養のため,増殖期と定常期の境が曖昧なので,接合型活性の誘導などには不向きだが,とにかく増えることは増える。また,つぎのような特徴もある。すなわち,滅菌した培養液では,かなりの富栄養のため細胞は急速に増えるが,また,急速に飢餓状態になる。一方,未滅菌の場合は,固形成分内の栄養分が徐々に溶出してくるので,急速に増えないかわりに,長期間手を加えずに培養を続けることができる。(ただし,雑菌の混入,空中からの胞子による鞭毛虫などの混入が起こるのは避けられない。雑菌が混入しても富栄養ではないので極端に培養が汚れることはないが・・・)
接合の誘導
交配反応による接合の誘導
1)試料の調整
上記の方法で,細胞を培養し,「接合型活性の強い細胞」を準備する。
そのためには・・・,
「ならし期間」が必要となる。
(時間の関係でここは未完成です)
接合型活性の強い細胞を得ることの難しさ
接合実験がうまくいくかどうかはここにかかっている!
現場の研究者は常にこれに悩まされている。
きれいに増えたからといって常に活性の強い細胞が得られるとは限らない。
抗生物質処理した直後のサンプルなどはきれいな培養液にいても
活性のない場合がある。
もともと活性の弱い株もいる。接合型活性の強い株を選んで実験に用いる。
簡単に失活し易い。温度,振動,コンタミ,酵素,
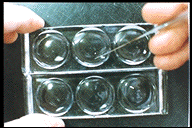
 交配反応の様子(左:混ぜる前,中:交配反応中,右:交配反応後にできた接合対)
交配反応の様子(左:混ぜる前,中:交配反応中,右:交配反応後にできた接合対)
2)接合型活性の維持のポイント
まず,実験に用いる細胞は,以下の接合型活性の出現条件を満たしていなければならない。
(文献参照)
- 成熟株である
- 培養の定常期にある
- 若過ぎない,古過ぎない
老化しても接合活性は維持される場合が多いが,未熟期をすぎたばかりの株
は接合型活性が強くないものが多い。
1〜3)の条件を満たしても活性がでない場合も多い。
考えられる原因:コンタミ(雑菌の混入)の影響
雑菌が混入したら必ずだめになるというわけではない。
通常は,接合活性には影響しない場合のほうが多い。
良いコンタミ;培養液表面に膜がはったような状態,試験管の壁面に白くついた汚れなどの
コンタミがあっても,培養液そのものが定常期に透明になるときは大丈夫な場合が多い。
悪いコンタミ;定常期に達しても培養液が白くにごるようなコンタミだとだめの場合がほとんど。
そのような場合,どうするか?
コンタミの除去
1)つまんで洗う
一般的には,この方法が一番確実(文献参照)
細胞を一匹ずつマイクロピペットでつまんで「洗う」
長所;うまくいくと完全に除去される。
欠点;操作に熟練を要す。時間がかかる(単離操作,増えるまでにも)
老化した株ほど成功率が下がる。「洗い」はうまくいっても
増えない場合が多くなる。
基本的に通常の室内で培養している限り,植え継ぎなどの際にコンタミする可能性が高い。
しかも,有菌培養なのでコンタミしてもすぐには気付かない。
きれいに洗ってもいずれは,再びコンタミする。この繰り返しが続く。
2)抗生物質処理
完全に除去するのは難しいが,接合活性のない場合など,大方の雑菌が除去されるだけで活性が回復する場合もある。
長所;簡便。熟練を要しない。
欠点;細胞にもダメージがある。強くすると死んだり,弱ってしまう。
回復に時間がかかる。処理後も丁寧に扱わないといけない。
=急にエサを多くやるとうまく増えないばあいもある。
与える量(=濃度)の調整が難しい。
コンタミの程度,種類により替えなくてはならない。
→詳しくは,「接合誘導」の解説文を参照
コツ;細胞が少ない場合,残された細胞を無駄にしない。
メモ:抗生物質の入手法について
医薬品として販売されている抗生物質は高価なうえに,購入するのに医師の許可証が必要になる。研究用の試薬として販売されているものは比較的易く自由に購入できる。
高率に接合を誘導する方法
接合過程を染色などで観察したり,接合対を単離するには,サンプルの中に接合対を形成していない細胞ができるだけ少ないほうが後々の処理が楽になる。
そのための高率に接合対を形成させる方法とは・・・
クランプ(交配反応による細胞凝集塊)に参加していないものを取り除く=上澄みを除去する。
それでも,クランプの中には接合活性の強いものと弱いものが混じってくる。(交配反応活性の弱い細胞が混じっていると,中には途中でクランプからはずれたり,接合対になるのが遅れるものが出てくる。)
同調して接合対を高率に誘導するためには,ドリル氏液などを小量加え,一度形成されたクランプを軽いピペッティングでくずし再度形成させる。
こうすると接合活性の弱い細胞の大部分はクランプに参加できずに浮いてくる。そこで,再び上澄みを除去してやれば,強い接合活性をもった細胞のみからなるクランプが残る。
接合過程のタイムコース(いつ減数分裂・受精・大小核の分化が起こるか)を調べる場合は,同調してないと意味がない。
接合対の単離法
注意:
0〜3時間後までは接合対は離れ易い。
3時間以降のサンプルから接合対の単離を行なうのがよい。
(途中)
接合の化学的誘導法
多くの株は,化学試薬処理で接合が誘導される(文献参照)。
被誘導能のない株もいる。(途中)
参考文献
A1. 原生動物細胞−医学生物学の実験系として− (1981)
野沢義則編 講談社サイエンティフック 講談社
(第4章 遺伝学的方法/月井雄二)
・・・・日本の ゾウリムシ・テトラヒメナ研究者による方法・研究成果の紹介書
A2. 微生物遺伝学実験法 石川辰夫 責任編集 (1982)
遺伝学実験法講座3 共立出版
(第13章 原生動物/月井雄二・樋渡宏一)
・・・・執筆したのは,上記の本よりも先,内容的にはほぼ同じ(13章)
A3. 生物材料調整法 江上信雄・勝見允行 編 (1982)
実験生物学講座1 丸善
(第7章 原生動物/茖原宏爾)
A4. 原生動物の観察と実験法 (1988)
重中義信 監修 共立出版
Copyright 1995-2008
原生生物情報サーバ
 交配反応の様子(左:混ぜる前,中:交配反応中,右:交配反応後にできた接合対)
交配反応の様子(左:混ぜる前,中:交配反応中,右:交配反応後にできた接合対)